Лихорадка: лечить или не лечить
Лихорадка, являющаяся одним из частых симптомов в клинической практике, помимо диагностических трудностей в расшифровке ее природы, требует у определенной категории пациентов ее купирования или ослабления проявлений, т.е. симптоматического лечения. Такие ситуации могут возникать у больных при наличии тяжелой сопутствующей патологии и риске ее декомпенсации на фоне лихорадки, а также в случаях индивидуальной плохой переносимости высокой температуры.
Негативные последствия повышения температуры тела до фебрильных цифр сводятся к следующим:
- тахикардия (повышение температуры на 1°С приводит к учащению ЧСС на 10-15 ударов в минуту);
- нарушения ритма, чаще экстрасистолия;
- повышение АД;
- повышенная потеря жидкости (за счет усиленного потоотделения и гипервентиляции);
- нарушения двигательной и абсорбционной активности кишечника;
- нарушения со стороны ЦНС (общемозговая симптоматика вплоть до развития спутанности сознания);
- активация латентной герпес-вирусной инфекции.
Указанные проявления могут оказывать особенно неблагоприятное воздействие на больных, страдающих различными сердечно-сосудистыми, неврологическими и другими заболеваниями.
Способы купирования лихорадки можно условно разделить на немедикаментозные и медикаментозные.
Среди немедикаментозных методов снижения температуры тела, имеющих особое значение в педиатрической практике, используют обтирание тела слабым раствором уксуса, влажные обертывания, теплые ванны, клизмы с водой комнатной температуры. Не следует укутывать больных (это препятствует теплоотдаче).
Медикаментозные способы купирования лихорадки основаны на знаниях и понимании механизмов повышения температуры тела при различных патологических процессах и заболеваниях. Повышение температуры тела происходит под воздействием эндогенных пирогенов (ИЛ-1, ИЛ-6, ФНО-a), которые воздействуют на нейроны переднего гипоталамуса посредством усиления синтеза простагландинов (ПГ) из арахидоновой кислоты.
Препараты, тормозящие синтез ПГ, применяют для купирования лихорадки или ослабления ее проявлений. Среди таких медикаментозных средств в клинической практике наиболее широко используются нестероидные противовоспалительные препараты (НПВП).
При принятии решения о назначении НПВП с целью купирования лихорадки врач должен отдавать себе отчет в том, что подобная терапия в данной ситуации носит исключительно симптоматический характер (если назначение НПВП не имеет целью достижение противовоспалительного эффекта, например, при артритах различного происхождения).
При этом потенциальный риск развития побочных эффектов даже при кратковременном приеме препаратов может превышать их жаропонижающий эффект. Поэтому принятие решения о назначении жаропонижающих средств должно быть взвешенным с учетом конкретной клинической ситуации, знаний особенностей фармакодинамики и фармакокинетики имеющихся в распоряжении врача препаратов.
Следует помнить о биологической целесообразности гипертермической реакции, а также о том, что отсутствие повышения температуры при инфекции свидетельствует о вероятности иммунодефицита и является неблагоприятным прогностическим фактором. Показаниями к назначению жаропонижающих средств являются не столько высокие цифры температуры тела, сколько ее плохая переносимость и риск возможного негативного влияния высокой температуры на различные органы и системы у больных с сопутствующей патологией и факторами риска.
Принятие решения о назначении жаропонижающего средства требует ответа на следующие вопросы:
- выбор препарата;
- путь введения;
- длительность применения.
При выборе препарата среди НПВП следует учитывать жаропонижающую активность, а также анальгетический эффект, поскольку болевые ощущения (головные боли, миалгии, артралгии и др.) нередко сопутствуют лихорадке. В таблице 1 представлены основные характеристики наиболее часто используемых НПВП, которые оцениваются в порядке убывания того или иного свойства.
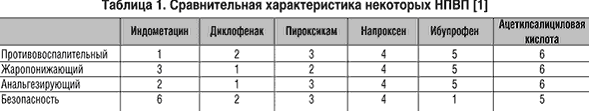
Кроме того, при выборе НПВП необходимо учитывать безопасность препарата, в том числе риск ульцерогенного эффекта, гепатотоксичность, цитопеническое действие, нефротоксичность, возможность взаимодействия с другими медикаментами, фармакокинетику препарата (длительность полувыведения, связь с белками, биодоступность и др.).
Путь введения НПВП должен обеспечивать оптимальную терапевтическую концентрацию препарата в крови, минимизировать риск побочных эффектов со стороны ЖКТ, быть удобным для применения и комфортным для пациента. С целью жаропонижающего эффекта используется прием препаратов внутрь, внутримышечные инъекции, внутривенные вливания и введение ректальных суппозиториев.
Пероральный прием НПВП является наиболее распространенным, но влечет за собой наибольший риск побочных эффектов со стороны ЖКТ (до 15%). Это зависит от продолжительности печеночной рециркуляции, определяющей длительность контакта со слизистой ЖКТ, что и приводит к гастроэнтерологической токсичности НПВП. С учетом этого при выборе перорального пути назначения НПВП предпочтение следует отдавать препаратам с коротким периодом полувыведения, быстрым всасыванием и быстрой элиминацией (ибупрофен, кетопрофен, диклофенак). Быстрая абсорбция способствует скорому наступлению жаропонижающего эффекта, а короткий период полувыведения снижает риск аккумуляции НПВП.
Внутримышечное (или внутривенное) введение НПВП с целью купирования или ослабления лихорадки широко практикуется врачами из-за более быстрого достижения жаропонижающего эффекта, а также в расчете на меньший риск гастроэнтерологической токсичности. Следует отметить, что различные побочные эффекты НПВП, в том числе и со стороны желудка, обусловлены не местным воздействием препарата, а ингибицией ЦОГ-1 независимо от способов введения их больному.
Вместе с тем при внутримышечном введении часто назначаемого диклофенака возможно развитие мышечных некрозов в местах инъекций, а при длительном внутримышечном введении увеличивается риск возникновения инфильтратов и абсцессов мягких тканей. Кроме того, применение инъекционных форм является экономически более затратным.
Лекарственные формы НПВП в виде ректальных суппозиториев имеют целый ряд преимуществ при применении их в качестве жаропонижающих средств:
- абсорбция лекарственного препарата через кровеносную и лимфатическую систему;
- отсутствие влияния пищи и других медикаментов на биодоступность НПВП;
- уменьшение риска побочных эффектов со стороны ЖКТ, особенно при патологии желудка, 12-перстной кишки;
- высокая биодоступность, сравнимая с таковой при внутримышечном введении.
Наличие в прямой кишке густой сети кровеносных и лимфатических сосудов способствует хорошей всасываемости с поверхности ее слизистой различных лекарственных веществ, которые через нижние геморроидальные вены попадают непосредственно в системный кровоток, минуя печень. При ректальном введении лекарственных препаратов удается избежать раздражающего действия на слизистую желудка. Для НПВП это имеет важное значение, поскольку большинство из них являются слабыми органическими кислотами, оказывающими наряду с системным влиянием на ЦОГ-1 локальный повреждающий эффект на желудок.
Время достижения максимальной концентрации НПВП при ректальном введении меньше по сравнению с пероральным приемом и приближается к таковой при внутримышечных инъекциях. Так, максимальная концентрация в крови при приеме внутрь 50 мг диклофенака достигается через 2-3 часа, в то время как при ректальном введении препарата - 30 минут.
Среди различных НПВП с целью жаропонижающего действия используются ректальные суппозитории диклофенка, кетопрофена, индометацина, напроксена.
Ректальные суппозитории Цефекон Н представляют комбинацию напроксена, салициламида и кофеина. Подобное сочетание обеспечивает достаточно выраженный жаропонижающий эффект и высокую анальгетическую активность. Входящий в состав суппозиториев Цефекона Н кофеин в дозе 50 мг значительно усиливает анальгетическое и жаропонижающее действие салицилатов и других НПВП, что, как полагают, связано с улучшением их биодоступности.
Невысокая доза напроксена (75 мг) в суппозитории Цефекон Н компенсируется наличием в препарате другого НПВП - салициламида (0,6 г). Более длительный период полувыведения напроксена (12-15 часов) по сравнению с салициламидом (5-6 часов) обеспечивает достаточно продолжительный жаропонижающий и анальгетический эффект Цефекона Н.
Продолжительность применения жаропонижающих средств определяется главным образом клинической ситуацией. В большинстве случаев, например, при ОРВИ, инфекциях ЛОР-органов длительность назначения НПВП для купирования лихорадки не превышает нескольких дней. В то же время у больных с различными бактериальными инфекциями при сохраняющейся лихорадке на фоне неэффективной антибактериальной терапии может сохраняться потребность в назначении НПВП.
Особое место занимают так называемые лихорадки неясного генеза, причина которых нередко остается нерасшифрованной в течение длительного времени, а сохраняющаяся лихорадка требует более продолжительного использования НПВП. В подобных ситуациях особое значение приобретает эффективность жаропонижающего действия, удобство применения и главное - безопасность используемого препарата.
Продолжительность непрерывного использования Цефекона Н, как и всех комбинированных анальгетиков, содержащих кофеин, не должна превышать 6 дней. Необходимость более длительного применения должно определяться клинической ситуацией (переносимость препарата, риск развития побочных эффектов, наличие и тяжесть сердечно-сосудистой, психоневрологической патологии и др.).
Таким образом, ректальные суппозитории Цефекон Н могут считаться оптимальным средством купирования лихорадки в различных клинических ситуациях, позволяя уменьшить риск побочных явлений со стороны ЖКТ и обеспечить поступление полной дозы независимо от приема пищи и сопутствующей терапии (антациды). Препарат обеспечивает выраженный и быстро наступающий жаропонижающий эффект, хорошо переносится, удобен в применении.
