Лечение бронхиальной астмы у детей
Бронхиальная астма (БА) – бронхолегочное заболевание, в основе которого лежат хроническое аллергическое воспаление стенки бронхов с участием различных клеток, особенно эозинофилов, лимфоцитов и тучных клеток, и бронхиальная гиперреактивность к различным стимулам. БА характеризуется периодически возникающими эпизодами бронхиальной обструкции, частично или полностью обратимыми, с приступообразным кашлем, свистящим дыханием, сдавлением в груди, экспираторной одышкой на различные специфические аллергические и неспецифические стимулы.
Отмечается увеличение распространенности БА, в различных регионах России она колеблется от 0,4 до 2%. Гипотезы, объясняющие возрастание частоты БА во всех возрастных группах, включают: увеличение воздействия воздушных поллютантов внутри жилища, связанное с особенностями современных строительных материалов и рециркуляцией воздуха; повышение содержания в воздухе диоксида азота и других раздражающих газов, воздействие аллергенов (особенно клещей домашней пыли, грибов, аллергенов животных, тараканов); увеличение частоты ранней заболеваемости респираторными вирусными инфекциями; выживаемость недоношенных детей с хроническими легочными заболеваниями; влияние курения матери на развитие легких ребенка; улучшение диагностики БА.
Факторы патогенеза
Хроническое аллергическое воспаление при БА развивается под воздействием комбинации различных медиаторов, высвобождающихся в результате реагинопосредованной реакции. У детей заболевание является проявлением атопии и нередко обусловлено наследственным предрасположением к гиперпродукции IgE. Ключевую роль в сенсибилизации организма играют CD4+ Tлимфоциты. Под воздействием аллергенных стимулов происходит активация и пролиферация Тh2субпопуляции CD4+ Тлимфоцитов с последующим выделением ими цитокинов (IL4, IL6, IL10, IL13), индуцирующих гиперпродукцию общего и специфических IgE.
Повторное поступление аллергена приводит к выделению клетками медиаторов после неспецифической стимуляции или связывания аллергенов с IgE на поверхности тучных клеток. Эти медиаторы (гистамин, лейкотриены С4, D4, Е4) вызывают развитие аллергического ответа, проявляющегося нарушением бронхиальной проходимости и приступом астмы. Бронхоспазм при раннем иммунном ответе ликвидируется b2агонистами и может быть предотвращен ингаляциями кромогликата и недокромила натрия.
Поздний иммунный ответ наблюдается спустя 68 часов, вызывает продолжительное состояние бронхиальной гиперреактивности с клеточной инфильтрацией слизистой оболочки эозинофилами, нейтрофилами. Для лечения на этой стадии и предотвращения поздней аллергической реакции необходимы кортикостероиды и превентивное назначение кромогликата или недокромила.
Развитие астмы связано с воздействием генетических и внешнесредовых факторов. Выделяют факторы:
- предрасполагающие к развитию БА (отягощенная аллергическими заболеваниями наследственность, атопия, бронхиальная гиперреактивность, неблагоприятная экология, табакокурение);
- причинные или сенсибилизирующие – способствующие появлению заболевания (аллергены, вирусные инфекции, лекарственные средства);
- вызывающие обострение (триггеры) путем стимуляции воспаления в бронхах и/или провоцирующие острый бронхоспазм (различные аллергены, вирусные и бактериальные инфекции, неспецифические воздействия, такие как холодный воздух, табачный дым, эмоциональный стресс, физическая нагрузка).
Наиболее важными в развитии сенсибилизации дыхательных путей являются ингаляционные аллергены (бытовые, эпидермальные, грибковые, пыльцевые). Ведущую роль в формировании бытовой аллергии играет домашняя пыль комплексный набор аллергенов, главным из которых является клещ домашней пыли, живущий в симбиозе с плесневыми грибами. Домашние животные один из сильнейших источников аллергенов (высокий уровень аллергенов сохраняется в течение нескольких лет). Аллергенами являются слюна, выделения, роговые чешуйки, слущенный эпителий. В последнее время все более частой причиной аллергических реакций становится аллерген тараканов.
Причиной развития пыльцевой БА могут быть аллергены трех основных групп растений деревья и кустарники, злаковые травы и сорные травы. У некоторых детей приступы удушья могут индуцировать различные лекарственные препараты: антибиотики, особенно пенициллинового ряда, сульфаниламиды, витамины, ацетилсалициловая кислота. Доказан вклад в развитие БА сенсибилизации к промышленным аллергенам. Под воздействием техногенного загрязнения атмосферного воздуха может изменяться структура и повышаться иммуногенность пыльцы и других аллергенов.
У детей разного возраста роль различных аллергенов в формировании БА неодинакова. Отмечается определенная последовательность развития сенсибилизации к различным аллергенам. Наиболее часто у детей первых лет жизни появляется пищевая и лекарственная аллергия, затем аллергия к бытовым, эпидермальным, грибковым аллергенам и с 34 лет более отчетливо пыльцевая сенсибилизация. Увеличивают риск появления астматических симптомов также ранние проявления атопии в виде атопического дерматита, воздействие пассивного курения.
Нередко первым провоцирующим обструктивный синдром фактором у детей являются респираторные вирусные инфекции, в последние годы повысилась роль хламидийной и микоплазменной инфекций. Вирусы (респираторно-синцитиальный вирус и вирус парагриппа) наиболее часто провоцируют бронхиальную обструкцию в раннем возрасте. После 3 лет более важное значение в развитии и обострениях заболевания приобретает риновирус. Один из механизмов их действия через стимуляцию афферентных вагальных рецепторов в дыхательных путях. Развитие бронхиальной обструкции при вирусных инфекциях может выявлять предрасположенность к БА, стимулируя IgEответ.
Обструкция дыхательных путей при БА развивается в результате бронхоконстрикции, гиперсекреции слизи, отека слизистой, клеточной инфильтрации и десквамации эпителия и воспалительных клеток. У больных с тяжелой фатальной астмой патологические изменения обнаружены в сегментарных и субсегментарных бронхах, с вовлечением мелких дыхательных путей, обычно респираторных бронхиол.
При этом отмечается утолщение базальной мембраны вследствие отложения коллагена IV типа, десквамация эпителия с потерей циллиарных клеток и частичной регенерацией бокаловидных и слизистых клеток, отек слизистой оболочки, гиперплазия и гипертрофия миоцитов, наличие в просвете воспалительных клеток (эозинофилов, лимфоцитов, тучных клеток, нейтрофилов). Патогномоничными являются кристаллы ШаркоЛейдена (лизофосфолипаза из мембран эозинофилов), спирали Куршмана (слепки слизи в просвете дыхательных путей) и тельца Креола (сгустки сладжированных эпителиальных клеток). Сходные, но менее выраженные изменения находят в дыхательных путях детей с менее тяжелыми формами заболевания.
Обструкция более выражена на выдохе, так как просвет внутригрудных дыхательных путей и в норме становится меньше во время выдоха. Увеличение внутрилегочного давления, необходимое для выдоха при обструкции дыхательных путей, нарастающая гиперинфляция сопровождаются увеличением работы дыхания и могут вызвать дальнейшее сужение и преждевременное закрытие дыхательных путей на выдохе. Увеличение внутригрудного давления изменяет венозный возврат, снижает сердечный выброс и ведет к появлению парадоксального пульса. Изменение соотношения вентиляции и перфузии, альвеолярная гиповентиляция ведут к нарушению обмена газов и нарастающей гипоксемии.
Клиническая картина
В конце XIX века известный российский педиатр Н.Ф. Филатов дал следующее описание клинической картины БА: ?Периодически повторяющиеся приступы сильной одышки с громким, тонким, высоким свистом в груди, слышным даже на расстоянии и сопровождающимся застоем венозной крови и цианозом. Западение уступчивых мест грудной клетки при вдыхании выражено не так резко, зато можно заметить признаки раздутия легких и усиление деятельности выдыхателей?.
У детей первых лет жизни БА может скрываться под маской респираторной вирусной инфекции с обструктивным синдромом, бронхиолита, обструктивного бронхита. В пользу БА свидетельствуют повторные (3 и более) рецидивы бронхиальной обструкции, уменьшение клинических проявлений под влиянием бронхолитической и противовоспалительной терапии, сочетание с отягощенной аллергическими заболеваниями наследственностью, с другими аллергическими заболеваниями.
Поскольку при многих других легочных заболеваниях могут присутствовать симптомы бронхиальной обструкции, кашель, наиболее значимыми для дифференциальной диагностики являются обратимый характер обструкции бронхов и наличие гиперреактивности бронхов.
У детей раннего возраста эквивалентами астмы могут быть эпизоды кашля в ночные или в предутренние часы (кашлевой вариант БА), от которых ребенок просыпается, повторный затяжной обструктивный синдром. В этих случаях состояние часто ошибочно расценивается, как обструктивный бронхит, рецидивирующий бронхит, астматический синдром и т.д.
Тяжесть течения БА определяется, исходя из клинических симптомов, частоты приступов удушья, потребности в спазмолитических препаратах, объективной оценки проходимости дыхательных путей по данным спирографии и пикфлоуметрии. Нередко врачом не используются четкие критерии тяжести заболевания, тяжесть оценивается субъективно, в медицинских документах отсуствуют конкретные данные, что приводит к завышению степени тяжести и трудностям в мониторировании эффективности терапии.
Частое сочетание БА и аллергического ринита (АР), сходство иммунопатологического ответа и хронического аллергического воспаления при этих нозологиях стало причиной появления концепции, что БА и АР манифестация единого заболевания верхних и нижних дыхательных путей. АР часто рассматривается, как фактор риска развития БА, а иногда и как ранняя стадия общего заболевания дыхательных путей. Верхние и нижние дыхательные пути функционально связаны: стимуляция слизистой носа через афферентные пути стимулирует парасимпатические волокна n.vagus, изменяя бронхомоторный тонус. У некоторых больных АР доминирует и БА не диагностируется или протекает субклинически, у других симптомы клинически выражены.
Ухудшить состояние больного с БА могут также синуситы. Инфицированные синусы представляют резервуар пролиферирующих бактерий. Эндотоксины из клеточной стенки грамотрицательных бактерий обладают провоспалительными свойствами, и показано, что ингаляции эндотоксина вызывают сужение дыхательных путей и гиперреактивность у больных с БА.
В диагностике важное место занимает исследование функции дыхания. У детей старше 5 лет и подростков проводится спирометрия. При БА определяется уменьшенная или нормальная форсированная жизненная емкость легких (ФЖЕЛ), уменьшение объема форсированного выдоха за 1 сек (ОФВ1), соотношения ОФВ1/ФЖЕЛ и пиковой скорости выдоха (ПСВ). Поскольку астматические проявления характеризуются эпизодичностью, вполне возможно, что при обследовании состояние легких может быть нормальным, особенно при легкой астме. Функцию дыхания исследуют также после ингаляции бронхолитика, физической нагрузки, провокационного теста с метахолином.
Метахолиновый тест проводится только при нормальных исходных показателях спирограммы. Более адекватным у детей является бронхолитический тест, при этом учитывается обратимость, т.е. прирост ОФВ1 и ПСВ на 12-15% (по некоторым данным, более 10%). Для мониторирования функции внешнего дыхания, эффективности терапии используется пифлоуметрия: определяется ПСВ и ее колебания в течение суток и под влиянием терапии; исследование проводится дважды в день (утром и вечером), при необходимости чаще.
У детей с атопической (экзогенной) БА после экспозиции различных аллергенов увеличена (но не всегда) концентрация как общего, так и специфических IgE к этим аллергенам, кожные пробы дают положительный ответ к различным аллергенам. У некоторых детей кожные пробы могут быть отрицательными, в том числе и при низкой концентрации IgE. Это вариант неатопической БА. Разделение между этими формами считается искусственным, так как основные иммунные нарушения и механизмы сходны в обеих группах. В последние годы повысился интерес к роли хламидийной и микоплазменной инфекции, которые также могут вызывать обструкцию. Однако концепция, что аллергические реакции к бактериям могут вызывать БА, не доказана.
Бронхиальная обструкция и свистящие хрипы являются наиболее характерными, но не патогномоничными для БА признаками. У детей первых месяцев жизни отмечается относительное преобладание врожденных и наследственных заболеваний, напоминающих по клинической картине БА.
К ним относятся: бронхиолит, аспирация инородного тела, муковисцидоз, циллиарная дисфункция, трахео и бронхомаляция, аномалии сосудов с компрессией дыхательных путей, стеноз, облитерирующий бронхиолит, бронхолегочная дисплазия, бронхогенные кисты, сердечная недостаточность. Полезными диагностическими методами являются рентгенография грудной клетки, компьютерная томография, контрастные исследования с барием, потовый тест, бронхо скопия с цитологическими и гистологическими исследованиями, бронхография.
Лечение
Лечебно-профилактическая тактика при БА определяется воспалительным характером процесса. Ведущими мерами являются элиминация аллеренов, применение препаратов, воздействующих на воспалительный процесс в бронхах, специфическая иммунотерапия. К симптоматической терапии относятся средства, улучшающие бронхиальную проходимость.
Базисная терапия
В лечении противовоспалительными препаратами используется принцип ступенчатой терапии, т.е. доза и количество применяемых средств возрастают по мере увеличения тяжести болезни или уменьшаются при ликвидации симптомов (рис. 1).
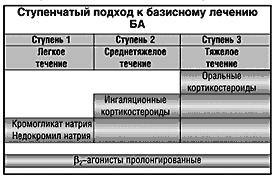
При легкой и среднетяжелой БА у детей назначают нестероидные противовоспалительные препараты: кромогликат натрия (интал) по 1–2 ингаляции 3–4 раза в день, с 2–х лет – недокромил натрия (тайлед) по 2 ингаляции 2–3 раза в день, в течение не менее 6–8 нед. Эти препараты используют также перед контактом с предполагаемым аллергеном или физической нагрузкой для предотвращения бронхоспазма.
У детей, особенно раннего возраста, у которых БА протекает на фоне кожной и интестинальной аллергии, назначают антигистаминные препараты (кетотифен, лоратадин, цетиризин и др.). Профилактическое использование антигистаминных препаратов уменьшает частоту обструктивного синдрома при ОРВИ, проявления аллергического ринита, выраженность сезонных симптомов БА.
Частое сочетание БА и аллергического ринита и риносинусита у детей ставит вопрос о целесообразности и обоснованности использования антигистаминных препаратов в этих случаях. Антигистаминные препараты стоят на первом месте в фармакотерапии аллергического ринита, уменьшая такие клинические симптомы, как зуд носа, чихание, ринорея, раздражение глаз и в меньшей степени блокаду носового дыхания. Н1-антагонисты в дозах, обычно используемых при сезонном АР, могут также улучшить конкурентные симптомы сезонной легкой астмы.
Современные антигистаминные препараты II и III поколения, не имеющие седативного эффекта, успешно применяются в комбинированной терапии БА и аллергического ринита у детей. Важным является использование адекватных доз и детских форм препаратов. Новая генерация антигистаминных препаратов, к которой относится фексофенадин (Телфаст), имеет более выраженную специфичность к Н1-рецепторам, чем антигистаминные препараты I поколения, и не обладает антихолинергическим и седативным эффектом, свойственным многим другим антигистаминным препаратам I и II поколения.
Показано, что фексофенадин эффективен при лечении умеренных и тяжелых симптомов сезонного АР. В России в 2002 г. зарегистрирована детская доза антигистаминного препарата III поколения фексофенадина (Телфаст 30 мг), назначаемая у детей с 6 лет по 1-2 таблетки в сутки.
У детей старше 6-7 лет могут быть использованы антилейкотриеновые препараты (зафирлукаст, монтелукаст), которые селективно блокируют рецепторы для лейкотриенов, обладающих бронхоконстрикторным эффектом. Точное место этих препаратов в программе лечения БА не определено, они могут применяться, как альтернативная терапия при нетяжелой БА или в комбинации с ингаляционными глюкокортикостероидами (ИГКС).
При сочетании БА и АР применение интраназальных глюкокортикоидов (беконазе, фликсоназе, назонекс) улучшает как симптомы АР, так и БА, уменьшает бронхиальную гиперреактивность. В тяжелых случаях возможно сочетание интраназальных и ингаляционных глюкокортикоидов, при этом общая доза не должна превышать рекомендуемый уровень.
При тяжелой БА и в случае недостаточной эффективности перечисленных средств при среднетяжелой БА препаратами базисной терапии являются ингаляционные глюкокортикостероиды (ИГКС). Применяют дозы ИГКС в зависимости от возраста и тяжести течения длительно, не менее 4-6 мес. Предпочтение у детей отдается минимальной эффективной дозе. Назначают беклометазона дипропионат, флютиказона пропионат, будесонид, флунизолид. В случае некупирующихся обострений доза ИГКС временно может быть удвоена. Побочное действие ИГКС по сравнению с пероральными глюкокортикоидами минимально, оно может проявляться при длительном использовании в дозах более 1000-1500 мкг/сут.
При сохраняющихся эпизодах одышки в течение дня и пробуждениях в ночные и предутренние часы назначаются пролонгированные бронхолитики (салметерол, формотерол, теопек) или комбинированные препараты. Комбинированная терапия (ИГКС совместно с пролонгированными b2агонистами или пролонгированными теофиллинами) применяется при длительном лечении БА для поддержания эффекта без дополнительного увеличения дозы. Среди пролонгированных бронхолитиков широко используется салметерол у детей уже с 4 лет (50 мкг 2 раза в сут).
Салметерол селективный b2агонист пролонгированного действия, с максимальным бронходилатирующим эффектом через 2 часа и длительностью действия 12 часов. Особенностью пролонгированного b2агониста формотерола является быстрое начало действия (через 13 мин) при длительности его 12 часов. Формотерол используют в виде препаратов Форадил (у детей старше 5 лет, по 12-24 мкг 2 раза в сутки) и Оксис турбухалер (у детей старше 12 лет по 4,5-9 мкг формотерола фумарата 2 раза в сутки).
Комбинации ИГКС и пролонгированных b2агонистов предназначены для регулярного лечения. Рациональность такой комбинации связана с комплементарностью действия компонентов. Пролонгированные b2агонисты и кортикостероиды взаимодействуют на молекулярном уровне. Кортикостероиды снижают десенситизацию и толерантность b2рецепторов, повышают их синтез в слизистой оболочке дыхательных путей. Пролонгированные b2агонисты стимулируют неактивный глюкокортикоидный рецептор, в результате чего он становится более чувствительным к стероидзависимой активации.
У детей с 4 лет используют Серетид, который сочетает комплементарную активность флютиказона пропионата и салметерола, оказывая противовоспалительное и бронхорасширяющее действие. Серетид представляет собой порошок, дозируемый с помощью ингалятора Мультидиска (каждая доза содержит 50 мкг салметерола ксинафоата в комбинации с 100 или 250 мкг флютиказона пропионата).
Серетид можно назначать детям с различной степенью тяжести БА при сохранении симптомов заболевания, несмотря на проведение терапии ИГКС, а также больным, у которых несмотря на регулярное применение бронходилататоров и кромонов имеется необходимость использования ИГКС. Показана хорошая переносимость и высокая эффективность этого препарата у детей. У детей старше 12 лет может использоваться также Симбикорт комбинация ИГКС будесонида (80 мкг или 160 мкг в 1 дозе) и пролонгированного бронхолитика формотерола (4,5 мкг в 1 дозе).
В фармакотерапии БА у детей используются также комбинации кромонов с b2агонистами короткого действия. Представителем этой группы является дитек дозированный аэрозоль, содержащий селективный b2агонист фенотерол (0,05 мг) и кромогликат натрия (1 мг).
Бронхолитическая терапия
Бронхолитическая симптоматическая терапия приводит к быстрому облегчению состояния. Бронхолитики у детей применяют по необходимости. Частая потребность (более 3-4 раз в сутки) является признаком недостаточного контроля за заболеванием и основанием для усиления противовоспалительной терапии. При приступе назначают b2агонисты короткого действия (сальбутамол, фенотерол). Препараты длительного действия (салметерол, формотерол) особенно эффективны для предотвращения ночных приступов удушья.
Метилксантины (эуфиллин, аминофиллин) оказывают спазмолитическое действие, действуют инотропно и предотвращают утомление респираторных мышц; продолжительность их действия 4-6 ч, средняя доза 5-7 мг/кг; назначаются они внутрь или внутривенно. Если ответ на аэрозоли бронхолитиков недостаточный, применяют эуфиллин внутривенно медленно. При выборе дозы необходимо учитывать назначение теофиллинов в предшествующие 4-5 часов. Безопасными считаются дозы, при которых достигается концентрация теофиллина в плазме 5-15 мкг/мл. В среднем доза теофиллина 1 мг/кг увеличивает его сывороточный уровень на 2 мкг/мл.
Способы ингаляционной терапии
При назначении ингаляционных препаратов следует уделять пристальное внимание технике проведения ингаляций это на 8090% определяет успех терапии.
В зависимости от возраста могут быть использованы различные способы ингаляционной терапии, улучшающие доставку препарата в легкие (спейсеры, небулайзеры, порошковые ингаляторы). Проблема синхронизации вдоха с моментом поступления лекарственного препарата является одной из самых важных при использовании дозированных аэрозольных ингаляторов. Не все дети оказываются в состоянии правильно освоить этот дыхательный маневр.
К современным эффективным способам доставки относится небулайзер, в котором распыление раствора препарата в форме влажного аэрозоля происходит с помощью сжатого воздуха, подаваемого компрессором или ультразвуковой энергии. При небулизации образуются частицы аэрозоля размером 25 мкм, оптимальные для поступления в дыхательные пути. Небулайзерная терапия может использоваться как в стационаре, так и в домашних условиях обученными родителями, она особенно показана детям раннего возраста.
Лечение обострения
Первичная помощь на амбулаторном этапе включает при легком/среднетяжелом обострении ингаляции b2агонистов короткого действия, лучше через спейсер большого объема (с лицевой маской у детей раннего возраста) до 10 ингаляций (1 вдох каждые 15-30 сек), или через небулайзер. При тяжелом приступе предпочтение отдается небулайзерной терапии.
Бронхоспазмолитики эффективно применяются в растворах через небулайзер особенно в первые годы жизни. Используют растворы сальбутамола, беродуала, сальгима, фенотерола. Сальбутамол используют в дозе 0,15 мг/кг (максимум 5 мг), при необходимости ингаляции повторяют с интервалом 2030 мин трижды в течение часа. Антихолинергический препарат ипратропиума бромид оказывает мягкое бронхолитическое действие, применяется для снятия острых нетяжелых приступов в дозе 0,25 мг, нередко в сочетании с b2агонистами (беродуал по 8-10 капель до 6 лет, 15-20 капель после 6 лет с 1,5-2,0 мл физиологического раствора).
При нарастающей тяжести заболевания, отсутствии ответа на терапию диагностируется астматический статус. Признаки тяжелого обострения: выраженная одышка, ребенок с трудом говорит, не может есть, число дыханий более 50/мин (более 40 у детей старше 5 лет), ЧСС более 140/мин (более 120 у детей старше 5 лет), участие вспомогательной мускулатуры, ПСВ менее 50% от должных или наилучших показателей (у детей старше 5 лет). Признаки, угрожающие жизни: цианоз, немое легкое, ослабление дыхания, общая слабость, у старших детей ПСВ менее 33%.
Для поддержания насыщения в артериальной крови кислородом (SaO2 более 92%) назначается оксигенотерапия (2-3 л/мин). Важным является поддерживающая уровень гидратации инфузия жидкости, эуфиллин 4-5 мг/кг в/в каждые 6 часов (0,75-1,25 мг/кг/час). Бронхоспазмолитики назначаются через небулайзер. Усиливает эффект b2агонистов назначение ипратропиума бромида через небулайзер по 0,25 мг каждые 6 часов.
У больных с тяжелой БА, получавших ранее кортикостероиды или находящихся на терапии ИГКС, в комплекс неотложных лекарственных назначений входят системные кортикостероиды коротким курсом. После назначения преднизолона в таблетках пик плазматической концентрации достигается через 12 часа. Некоторые эффекты преднизолона (в таблетках или в/в) отмечаются через 2 часа (снижение эозинофилов и лимфоцитов в периферической крови), другие через 6-8 часов (улучшение легочной функции). Назначается преднизолон внутрь (до 1 года 12 мг/кг/сут, в возрасте 15 лет по 10-20 мг/сут) или парентерально каждые 6 часов. Хороший эффект для купирования обострения оказывают ингаляции через небулайзер будесонида (Пульмикорт) ингаляционного кортикостероида, который применяется в дозе 0,5-1,0 мг/сут.
Адреналин при БА в настоящее время используется редко изза побочных эффектов препарата его заменили дозированные аэрозоли бронхолитиков. Он может быть использован при резком снижении инспираторного потока в дозе 0,01 мл/кг в концентрации 1:1000 (не более 0,3 мл в любом возрасте для минимизации побочных эффектов) однократно или дважды с интервалом в 20 мин.
Специфическая иммунотерапия
Специфическая иммунотерапия относится к базисной терапии легкой и среднетяжелой астмы, проводится в стадии ремиссии аллергологом. Иммунотерапия аллергенами (аллерговакцинация) составляет важный терапевтический раздел в лечении БА и АР. Иммунотерапия может изменять естественное течение заболевания и сохранять эффект на многие годы после ее прекращения.
Образовательные программы
Большую роль в терапии БА играет образование пациентов и родителей. Информация о заболевании, принципах терапии, поведении во время приступа, получаемые в беседе с врачом или на занятиях в астма-школах, помогают бороться с заболеванием.
Профилактика
В связи с многообразием факторов, участвующих в развитии заболевания профилактика БА представляет существенные проблемы. Важное значение имеют улучшение экологической ситуации, в том числе экологии жилища, снижение заболеваемости вирусными инфекциями, профилактика аллергических воздействий, начиная с периода внутриутробного развития, уменьшение экспозиции аллергенов и воздействия курения (в том числе пассивного), грудное вскармливание.
